Publikacje
Recenzowane artykuły przypadków klinicznych
Techniki robotyczne i wspomagane laserowo w chirurgii urologicznej: aktualne zastosowania
Robotic and Laser-Assisted Techniques in Urologic Surgery: Current Applications
ChirurgiaMetody Ten narracyjny przegląd literatury został przeprowadzony przez systematyczne przeszukiwanie internetowych baz danych, w tym PubMed, Scopus i Cochrane Library pod kątem publikacji między styczniem 2018 r. a majem 2025 r. Główny nacisk skupiono się na klinicznych zastosowaniach robotycznych i laserowych technik chirurgicznych w urologii. technik chirurgicznych w urologii. Strategia wyszukiwania obejmowała słowa kluczowe i operatory logiczne, takie jak: "chirurgia zrobotyzowana" ORAZ "urologia", "enukleacja laserowa" LUB "HoLEP" LUB "PVP", "minimalnie inwazyjna" ORAZ "rak urologiczny", "prostatektomia wspomagana przez robota" LUB "prostatektomia wspomagana przez robota". prostatektomia" LUB "nefrektomia nefrektomia". Kryteria włączenia były następujące: - recenzowane badania, próby kliniczne, metaanalizy i przeglądy systematyczne. - Publikacje w języku angielskim. - Badania z udziałem dorosłych pacjentów poddawanych zabiegom urologicznym. - Nacisk na zabiegach z użyciem robota lub lasera. Kryteria wykluczenia były następujące: - opisy przypadków opisy przypadków, listy do redakcji lub artykuły redakcyjne bez danych. - Publikacje nieanglojęzyczne publikacje. - Badania skoncentrowane wyłącznie na populacjach weterynaryjnych lub pediatrycznych (z wyjątkiem przypadków istotne dla urologii robotycznej). Zidentyfikowano łącznie 137 artykułów. Po sprawdzeniu tytułów i streszczeń, przejrzano 68 artykułów pełnotekstowych, a 38 badań zostało w oparciu o istotność, jakość metodologiczną i aktualność. aktualności. Głównymi analizowanymi punktami końcowymi były czas operacji, szacowana utrata krwi (EBL), długość pobytu w szpitalu, wskaźniki powikłań i wyniki funkcjonalne. wyniki funkcjonalne. Drugorzędowe punkty końcowe obejmowały analizę kosztów i implikacje etyczne. Zabiegi urologiczne wspomagane robotem Chirurgia wspomagana robotem zrewolucjonizowała dziedzinę urologii, zwiększając precyzję, minimalizując inwazyjność i poprawiając wyniki pooperacyjne. wyniki pooperacyjne. System chirurgiczny da Vinci, zatwierdzony przez FDA w 2000 roku, pozostaje najczęściej stosowaną platformą. 2000 roku, pozostaje najczęściej stosowaną platformą. Platformy robotyczne umożliwiają trójwymiarowe widzenie w powiększeniu, większą artykulację instrumentów i lepszą ergonomię. ulepszoną ergonomię, z których wszystkie mają kluczowe znaczenie dla złożonych zabiegów miednicy i zaotrzewnowych. i zaotrzewnowych. Radykalna prostatektomia zrobotyzowana (RARP) Radykalna prostatektomia jest jednym z najbardziej uznanych zabiegów zrobotyzowanych w urologii. zabiegów zrobotyzowanych w urologii. Radykalna prostatektomia wspomagana robotem (RARP) w dużej mierze zastąpiła techniki otwarte i laparoskopowe ze względu na doskonałą wizualizację wiązek nerwowo-naczyniowych oraz poprawę trzymania moczu i erekcji w niektórych kohortach (1). Liczne badania wykazują porównywalną kontrolę onkologiczną między RARP a operacją otwartą, ze znacznie zmniejszoną utratą krwi, niższymi wskaźnikami transfuzji i krótszą hospitalizacją(2) . i krótszą hospitalizacją(2). Innowacje, takie jak systemy z podwójną konsolą i algorytmy oszczędzające nerwy jeszcze bardziej poprawiają wyniki pacjentów. Zrobotyzowana nefrektomia częściowa i radykalna Zrobotyzowana nefrektomia częściowa (RPN) jest uważana za standard w przypadku małych guzów nerek. w przypadku małych guzów nerek ze względu na zalety oszczędzania nefronów. Podejście robotyczne umożliwia precyzyjne wycięcie guza przy minimalnym czasie ciepłego niedokrwienia i lepsze zszycie ubytku nerki(3). W porównaniu do laparoskopowej częściowej nefrektomii nefrektomii, RPN wykazuje niższe wskaźniki konwersji i lepszą pooperacyjną funkcję nerek(4). nefrektomia radykalna, choć rzadziej stosowana niż nefrektomia częściowa, jest korzystniejsza niż nefrektomia laparoskopowa. częściowa nefrektomia, jest korzystna w wybranych przypadkach złożonych lokalizacji guza lub dużych mas nerkowych. lub dużych mas nerkowych.
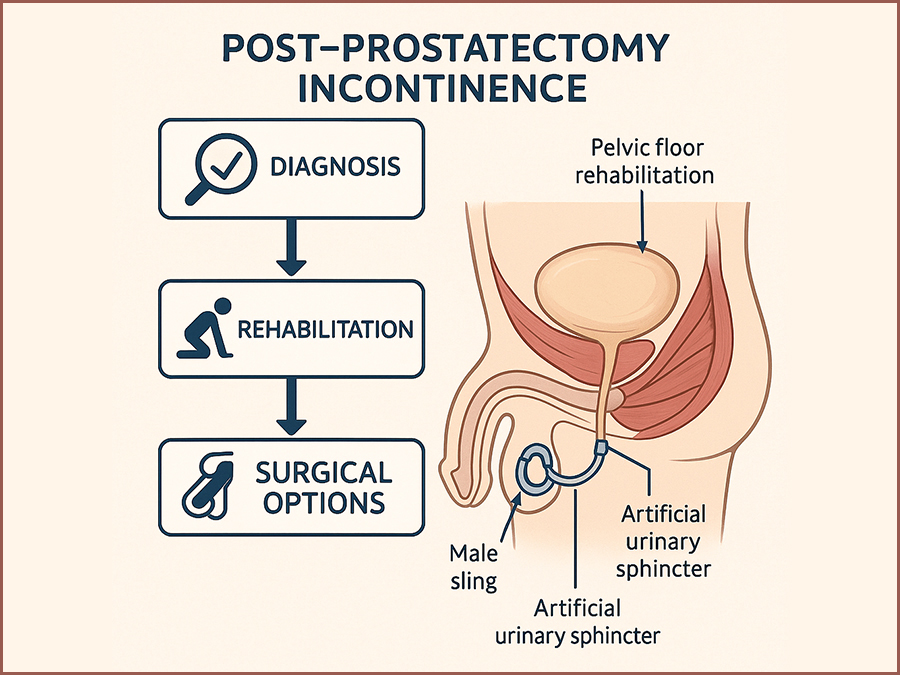
Nietrzymanie moczu po prostatektomii: czynniki ryzyka, rehabilitacja i opcje chirurgiczne
Post-Prostatectomy Incontinence: Risk Factors, Rehabilitation, and Surgical Options
ChirurgiaRadykalna prostatektomia jest Kamień węgielny terapii leczniczej zlokalizowanego raka prostaty, oferujący korzystne wyniki onkologiczne u odpowiednio dobranych pacjentów. Jednakże, jednym z najczęstszych i najbardziej niepokojących powikłań jest nietrzymanie moczu po prostatektomii (PPI). nietrzymanie moczu po prostatektomii (PPI), przy czym zgłaszane wskaźniki wahają się od 4% do 40% w zależności od w zależności od zastosowanej definicji, techniki chirurgicznej i czasu oceny. (1,2) Powikłanie to znacząco wpływa na jakość życia związaną ze zdrowiem, powodując dyskomfort fizyczny, emocjonalny i wycofanie społeczne. emocjonalny i wycofanie społeczne.(3) PPI różni się od innych rodzajów nietrzymania moczu u mężczyzn nietrzymania moczu u mężczyzn zarówno pod względem etiologii, jak i postępowania. Wynika to przede wszystkim z jatrogennego uszkodzenia mechanizmu zwieraczowego podczas usuwania prostaty, chociaż dodatkowe czynniki przyczyniające się obejmują nadaktywność wypieracza, i zmiany w dynamice szyi pęcherza moczowego.(4,5) Pomimo postępów w minimalnie inwazyjnych i robotycznych metodach chirurgicznych i zrobotyzowanych podejść chirurgicznych, PPI pozostaje wyzwaniem zarówno dla pacjentów, jak i klinicystów. i klinicystów. Kompleksowe zrozumienie patofizjologii i czynników ryzyka PPI jest niezbędne do opracowania optymalnych strategii zapobiegania i leczenia. strategii zapobiegania i zarządzania. Ponadto, klinicyści muszą być dobrze zorientowani zarówno w niechirurgicznych, jak i chirurgicznych metodach leczenia, aby dostosować terapię do indywidualnych potrzeb i oczekiwań pacjenta. terapię do indywidualnych potrzeb i oczekiwań pacjenta.(6,7) Niniejszy przegląd ma na celu syntezę aktualnych dowodów na temat PPI, koncentrując się na możliwych do zidentyfikowania czynnikach ryzyka, skutecznych strategiach rehabilitacyjnych skutecznych strategiach rehabilitacyjnych i dostępnych metodach leczenia chirurgicznego. Poprzez konsolidację współczesnych badań i wytycznych klinicznych, niniejszy artykuł ma na celu zapewnienie jasnych ram postępowania z PPI w praktyce urologicznej.
Infekcja COVID-19 imitująca ostrą białaczkę promielocytową
COVID-19 infection mimicking acute promyelocytic leukemia
ChirurgiaOstra białaczka promielocytowa (ang. acute promyelocytic leukemia, APL) jest podtypem ostrej białaczki szpikowej (ang. acute myeloid leukemia, AML), u której podłoża leży blok różnicowania na szczeblu promielocyta, za co w 95% przypadków odpowiedzialna jest translokacja między chromosomem 15 a 17, t(15;17)(q22,q21), w wyniku której dochodzi do fuzji genów PML i RARA. W rezultacie produkowane jest białko fuzyjne PML-RARα, którego obecność prowadzi do samoodnowy i zahamowania różnicowania komórek z linii mieloidalnej na etapie promielocyta [1, 2]. Rozpadające się promielocyty uwalniają ziarnistości o właściwościach tromboplastycznych, co skutkuje indukcją zespołu wykrzepiania wewnątrznaczyniowego (ang. disseminated intravascular coagulation, DIC), z wtórną fibrynolizą i wysokim ryzykiem śmiertelnych powikłań krwotocznych [3]. Rozpoznanie APL stawiane jest na podstawie objawów klinicznych, wyników morfologii krwi obwodowej, cytometrii przepływowej i badań szpiku obejmujących badania cytogenetyczne i molekularne. W mielogramie stwierdza się obecność nieprawidłowych morfologiczne promielocytów zawierających w cytoplazmie charakterystyczne ziarnistości, tzw. pałki Aurea. W badaniu cytometrycznym analizowane komórki szpiku cechują się wysoką ekspresją antygenów CD13, CD33 oraz niską lub brakiem ekspresji antygenów CD11b, CD34, CD117, HLA-DR. W celu rozpoznania APL niezbędne jest jednak wykazanie obecności translokacji t(15;17) metodą FISH lub białka PML-RARα metodą RT-PCR lub innych typowych, rzadziej występujących rearanżacji genu RARα [1, 4]. Ze względu na duże ryzyko rozwoju zespołu DIC oraz związane z tym wysokie ryzyko zgonu pacjenta leczenie przeciwnowotworowe włącza się już w przypadku podejrzenia APL, czyli przed otrzymaniem wyników potwierdzających translokację t(15;17) i/lub rearanżację genu PML-RARα. Leczenie opiera się na zastosowaniu kwasu all-trans retinowego (ang. all-trans retinoic acid, ATRA), który wpływa na konformację nieprawidłowego białka fuzyjnego PML-RARα, co w rezultacie prowadzi do indukcji różnicowania i dojrzewania promielocytów [1, 5]. Infekcja COVID-19 jest wciąż słabo poznaną jednostką chorobową. Przebieg infekcji, jej powikłania oraz skutki odległe nie są w pełni znane. W pewnych przypadkach można podejrzewać, iż przyczynia się ona do zaburzeń procesu hematopoezy, skutkując zaburzeniem dojrzewania różnych linii komórkowych. Infekcja Covid-19 może między innymi doprowadzić do namnożenia komórek blastycznych we krwi lub szpiku, sugerując nawet rozpoznanie ostrej choroby rozrostowej [6]. Przedstawiamy przypadek pacjentki, u której w trakcie infekcji COVID-19 wystąpiły zaburzenia hematologiczne imitujące ostrą białaczkę promielocytową.
Postępowanie w dystocji barkowej u pacjentki rodzącej do wody - studium przypadku
The management in shoulder dystocia during water birth- case study.
GinekologiaPraca dotyczy postępowania w dystocji barkowej u kobiety rodzącej do wody. Zawiera wytyczne postępowania podczas dystocji barkowej opracowane w Katedrze i Oddziale Klinicznym Ginekologii i Położnictwa w Tychach.
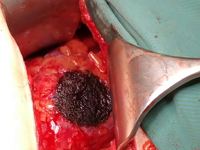
Zastosowanie technologii water i koagulacji plazmą argonową w chirurgii organooszczędzającej guza nerki – opis przypadku
Application of water jet technology and argon plasma coagulation in nephron-sparing surgery for a kidney tumour – a case report.
ChirurgiaDzięki Ze względu na coraz większą rolę obrazowania medycznego (np. ultrasonografii, tomografii komputerowej lub rezonansu magnetycznego), liczba przypadkowo wykrytych tomografia komputerowa lub rezonans magnetyczny), rośnie również liczba przypadkowo wykrytych guzów nerek. guzów nerek również rośnie. Guzy te są zwykle małymi guzami nerek (SRM) we wczesnych stadiach zaawansowania (1). Zgodnie z wytycznymi Europejskiego Towarzystwa Urologicznego, guzy nerek we wczesnych stadiach zaawansowania (T1) powinny być leczone z oszczędzeniem nefronów (NSS). W dłuższej perspektywie ten rodzaj pozwala na zachowanie funkcji nerek, zmniejsza ogólną śmiertelność i zmniejsza częstość występowania zdarzeń sercowo-naczyniowych (2). Głównymi celami NSS są usunięcie guza z ujemnymi marginesami chirurgicznymi i zachowanie jak najlepszej funkcji pozostałego miąższu nerki przy zminimalizowanym ryzyku zdarzeń niepożądanych. zdarzeń niepożądanych. Postęp technologii medycznych sprawia, że chirurgiczne są coraz bardziej skuteczne.
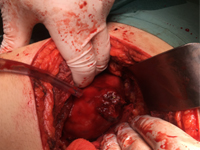
Zespół Wunderlicha objawiający się samoistnym krwotokiem nerkowym w jamie zaotrzewnowej jako pierwsza manifestacja raka nerkowokomórkowego
Wunderlich Syndrome presenting as Spontaneous renal haemorrhage in the retroperitoneal cavity as the first manifestation of renal cell carcinoma.
ChirurgiaSpontaniczny, nieurazowy krwotok zaotrzewnowy lub zespół Wunderlicha (WS) jest rzadkim, ale potencjalnie zagrażającym życiu stanem. Może okazać się śmiertelny, jeśli nie zostanie rozpoznany i leczony agresywnie w odpowiednim czasie. Wstrząs spowodowany masywnym krwotokiem zaotrzewnowym lub śródotrzewnowym może wystąpić w pojedynczych przypadkach [1]. Wyniki kliniczne nie są specyficzne, dlatego w diagnostyce różnicowej należy uwzględnić wiele łagodnych i złośliwych guzów nerek do czasu postawienia prawidłowej diagnozy przez patologa. Obrazy TK i USG nie są charakterystyczne. Najczęstszą przyczyną krwawienia jest angiomiolipoma. Rzadziej jest to polekowe zapalenie naczyń, rak nerki, guz chromochłonny lub torbiel nerki. Przedstawiamy przypadek 53-letniego mężczyzny z objawami krwotoku nerkowego w jamie zaotrzewnowej jako pierwszej manifestacji raka nerkowokomórkowego.
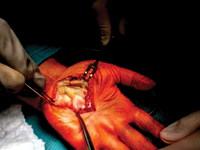
Izolowany nerwiakowłókniak splotowy ręki: opis dwóch przypadków. Propozycje diagnostyki i leczenia.
Isolated hand plexus neurofibroma: two case reports. Diagnostics and treatment proposals.
GinekologiaNerwiakowłókniaki splotowe są łagodnymi nowotworami osłonki nerwów obwodowych. Można je spotkać jako guzki pojedyncze lub mnogie, będące częścią obrazu klinicznego w dowolnym typie neurofibromatozy, mogące ulec zezłośliwieniu. Nerwiakowłókniaki powstają z komórek Schwanna wchodzących w skład nerwów skóry całego ciała, nerwów unerwiających narządy wewnętrzne i nerwów czaszkowych. Do najbardziej charakterystycznych objawów należy obecność rozproszonych, wydłużonych, sprężystych guzków podskórnych. Są to włókniaki, histologicznie przypominające pojedyncze nerwiaki, pojawiające się wzdłuż przebiegu nerwów obwodowych lub nerwów czaszkowych. Najczęściej występują na twarzy i szyi. Czasami prowadzą do masywnego powiększenia kończyny lub innej części ciała (słoniowacizna neurofibromatyczna) [1,2]. Innym, równie często spotykanym objawem są przebarwienia skórne, wyglądem przypominające plamy kawowe ("giant café-au-lait spot"), a także zmiany o charakterze piegów lokalizujące się w okolicach pachwin oraz dołów pachowych [3]. Objawy neurologiczne związane są z uciskiem nerwiakowłókniaków na struktury sąsiadujące. Chory uskarża się wtedy na nerwobóle nerwów obwodowych. W literaturze możemy spotkać pojedyncze przypadki neurofibroma plexiform bez jakiegokolwiek związku z neurofibromatozą typu 1 [4-6]. Leczenie pacjentów z nerwiakowłókniakami splotowymi nie jest dobrze zdefiniowane i ma na celu głównie kontrolowanie objawów. Chirurgiczne wycięcie jest jedyną dostępną terapią, gdyż nie ma leków, które mogłyby zapobiegać ich powstawaniu lub leczyć je zachowawczo. W chwili obecnej wyniki chirurgicznego wycięcia nie są w pełni zadowalające, a procedury te mogą być skomplikowane ze względu na rozmiar, lokalizację, stan naczyń, zaangażowanie nerwowe, mikroskopowe utkanie i wysokie tempo ponownego wzrostu guza [7]. Należy również wziąć pod uwagę fakt , iż znanych jest wiele przyczyn wywołujących zmiany guzowate podobne do nerwiakowłókniaków . Obejmują one urazowe uszkodzenia tkanek miękkich, zapalenia stawów, choroby ścięgien (np. tendinoza, zapalenie pochewki ścięgna, zerwanie ścięgna), nienowotworowe zmiany tkanek miękkich (np. ganglion, zapalenie kaletki, ziarniniak) , oraz rzadziej nowotwory i ich przerzuty do tkanek miękkich [8]. Ogniskowe zmiany tkanek miękkich są często przyczyną bólu i wyczuwalnej masy guza [9]. W przypadkach tych, zwłaszcza w początkowym okresie, trafna diagnostyka jest kluczowa, aby ustalić rozpoznanie i strategię leczenia. Dlatego w konfrontacji z ogniskową zmianą guzowatą logicznym wydaje się przestrzeganie ustalonego algorytmu postępowania. Najpierw powinno się zapewnić dokładny opis zmiany w korelacji z wiekiem pacjenta, lokalizacją, rodzajem zajętej tkanki, stanem sąsiadującego otoczenia. W tym celu, oprócz szczegółowego badania klinicznego należy wykonać USG zajętego obszaru, a jeżeli podejrzewamy zmianę kostną to bad. rtg w dwóch projekcjach z sąsiadującymi stawami. Zaawansowanie zmian kostnych, wymusza pogłębienie diagnostyki poprzez badanie TK. Natomiast zmiana ograniczona tylko do tkanek miękkich w USG wymagać będzie diagnostyki MRI, co dokładniej zobrazuje infiltrację przez nią sąsiedztwa. Jeżeli badania obrazowe wykażą wysokie prawdopodobieństwo choroby rozrostowej, istotnym elementem diagnostycznym jest uzyskanie materiału do badania patomorfologicznego, pobranego w trakcie biopsji otwartej lub oligobiopsji i ustalenie rozpoznania histologicznego [10]. W przypadku potwierdzenia procesu nowotworowego konieczne zawsze jest wykonanie badania RTG/TK klatki piersiowej, USG/TK jamy brzusznej, a nawet PET celem wykluczenia przerzutów [11]. Drugi etap wdrożonego algorytmu nakazuje zaplanować leczenie w oparciu o odpowiedzi na następujące pytania: - Czy zmiana może być normalnym wariantem, czyli „zostaw mnie w spokoju, nie dotykaj”, uszkodzenie łagodnego typu, nie wymagające dalszego obrazowania i zaopatrzenia, a tylko obserwacji? [12] - Czy zmiana ma cechy sugerujące agresywną naturę, a wtedy jak daleko zaawansowane powinno być leczenie? [13]. Niejednorodność obrazu klinicznego niezidentyfikowanych ogniskowych zmian guzowatych w okolicy śródręcza, różnorodność dostępnych metod diagnozowania nie ułatwiają zadania, zarówno na etapie stawiania wstępnego rozpoznania, jak i podczas komunikacji między członkami zespołu interdyscyplinarnego, który niejednokrotnie powinien zająć się leczeniem. Dlatego też wydaje się ważną być współpraca na linii ortopeda-onkolog-patomorfolog. Dwa przypadki izolowanej nerwiakowłókniakowatej zmiany dłoniowej części ręki opisane zostały poniżej ze względu na ich unikalność. Drugi z opisanych przypadków wskazał na dodatkową możliwość pozabiegowego doleczania pacjenta pod postacią inejkcji proloterapeutycznych poprawiających wydolność leczonej kończyny.
Wybrane odrębności w żywieniu dzieci w trakcie leczenia onkologicznego. Cykl: Leczenie żywieniowe — ab ovo.
Selected differences in nutrition of children during oncological treatment. Nutrition therapy - editorial cycle.
InneLeczenie onkologiczne związane jest z dużym ryzykiem niedożywienia u dzieci. Powikłania leczenia często unieumożliwiają spożywanie pokarmów doustnie, co wymaga odpowiedniej modyfikacji żywienia i rozważenia żywienia pozajelitowego.
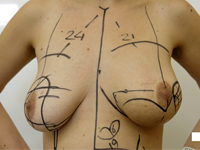
Mastektomia i jednoczasowa rekonstrukcja piersi u chorej na mięsaka gruczołu po przebytym skojarzonym leczeniu oszczędzającym z powodu raka
Mastectomy and immediate reconstruction at woman with breast sarcoma following breast connserving treatment due to cancer
GinekologiaMięsaki piersi występują rzadko, stanowiąc 1% złośliwych nowotworów gruczołu i mniej niż 5% wszystkich nowotworów mezenchymalnych.1 Niska zapadalność utrudnia przeprowadzenie badań klinicznych z randomizacją, a dostępne dane obejmują opisy retrospektywnych serii i pojedynczych przypadków. Liczba znanych czynników, zwiększających ryzyko zachorowania jest niewielka. Predyspozycja genetyczna w postaci zespołu Li-Fraumeni (mutacji genu TP53) zwiększa ryzyko pojawienia się pierwotnych mięsaków także w lokalizacji piersiowej.2 Przewlekły obrzęk chłonny pojawiający się u części pacjentek po limfadenektomii pachowej i napromienianiu pachy predysponuje do wystąpienia chłoniakomięsaka (lymphangiosarcoma) w obrębie zmienionego ramienia (zespół Stewarta i Trevesa).3 Mięsaki wtórne pojawiają się sporadycznie w piersiach uprzednio napromienianych po zabiegach oszczędzających (BCT – ang. breast conserving treatment), wykonywanych z powodu raka gruczołu piersiowego, najczęściej występującego nowotworu złośliwego u kobiet, oraz po radioterapii prowadzonej z powodu ziarnicy złośliwej.4 Skumulowane ryzyko wystąpienia mięsaka indukowanego radioterapią (RIS – ang. radiotherapy induced sarcoma) wynosi 3,2 na 1000 w ciągu 15 lat w porównaniu do 2,3 na 1000 dla pierwotnego mięsaka w populacji bez radioterapii.5 W porównaniu do kobiet, które nie były napromieniane, u chorych leczonych radioterapią z powodu raka piersi ryzyko zachorowania na naczyniakomięsaka indukowanego radioterapią (ang. radiotherapy induced angiosarcoma, RIA) jest pięciokrotnie wyższe 6 , generalnie jednak możliwość wystąpienia mięsaka po przebytej radioterapii jest niska i według danych z literatury wynosi ona 0,03 - 0,2% w ponad 10-letniej obserwacji.7,8 Należy wyraźnie podkreślić korzyści odnoszone przez kobiety chore na raka piersi dzięki napromienianiu, będącego obligatoryjną częścią leczenia oszczędzającego pierś.9 Nie wykazano korelacji występowania RIS ze stosowaniem chemioterapii.10 Do rozpoznania mięsaka wyindukowanego radioterapią można zastosować kryteria zaproponowane przez Cahana w 1948 r.11 w interpretacji Kirovej15 (Cahan opisał wówczas kilkanaście przypadków mięsaków kości u pacjentów napromienianych zgodnie z ówczesnymi standardami leczenia z powodu łagodnych zmian i gruźlicy kości, pierwszym punktem w oryginalnym opisie był nienowotworowy charakter leczonej radioterapią zmiany)11: 1. leczenie w przeszłości napromienianiem 2. bezobjawowy okres utajenia między dwoma nowotworami trwający kilka lat 3. wystąpienie mięsaka we wcześniej napromienianym obszarze, 4. histopatologiczne potwierdzenie mięsaka jako drugiego nowotworu.10,11,15 Jakkolwiek Cahan określił okres utajenia jako “relatywnie długi“, wynoszący w jego pracy ponad 5 lat, w piśmiennictwie opisano przypadek, który pojawił się przed upływem roku, również określony jako RIS (RIA).12 Do typów histopatologicznych rozpoznawanych wśród wtórnych mięsaków należą: angiosarcoma, hemangiosarcoma, leiomyosarcoma, malignant fibrous histiocytoma, liposarcoma, fibrosarcoma. Opisywano także chondrosarcoma i osteosarcoma. RIS rozwijają się najczęściej w ścianie klatki, rzadziej w miąższu napromienianej piersi.10 Metodą z wyboru w przypadku chorych na mięsaki piersi jest wycięcie guza z marginesem zdrowych tkanek. O ile w przypadku pierwotnych mięsaków leczenie uzupełniające po zabiegu oszczędzającym polega często na napromienianu okolicy operowanej, w przypadku leczenia chorych na mięsaka występującego w polu uprzednio napromienianym powtórna radioterapia tego samego obszaru nie jest zalecana. Optymalnym rodzajem zabiegu jest w takim wypadku mastektomia.
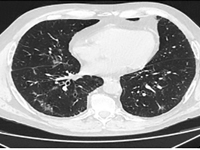
Infekcja SARS-CoV-2 u chorego na raka gruczołowego z mutacją w genie EGFR leczonego erlotynibem – opis przypadku
SARS-CoV-2 infection in a patient with adenocarcinoma with a mutation in the EGFR gene treated with erlotinib - a case report
InternaRak płuca odpowiada za największą liczbę zgonów z powodu nowotworów na świecie [1]. Pomimo postępów w leczeniu wskaźniki zachorowalności i śmiertelności wciąż wzrastają. Analiza GLOBOCAN z 2018 roku zaraportowała 2,09 milionów nowych przypadków zachorowań na raka płuca i 1,76 milionów zgonów z powodu raka płuca na świecie [2]. Rozróżnia się dwa główne typy histologiczne: drobnokomórkowy rak płuca (DRP) oraz niedrobnokomórkowy rak płuca (NDRP). NDRP stanowi około 85% wszystkich przypadków raka płuca. Obejmuje różne podtypy, takie jak rak gruczołowy, rak płaskonabłonkowy i rak wielkokomórkowy. Najczęściej występującym podtypem jest rak gruczołowy stanowiący 45% przypadków NDRP. Najważniejszym czynnikiem ryzyka rozwoju raka płuca jest palenie, szczególnie wśród populacji męskiej. Używanie papierosów z filtrem, który obniża ilość substancji smolistych dostających się do płuc, koreluje ze wzrostem zachorowań na gruczolakoraka płuc, co związane jest silniejszą inhalacją karcynogenów do drobnych dróg oddechowych. Inne związki mogące wywierać wpływ na rozwój nowotworu stanowią azbest, radon, nikiel, kadm, chrom, krzemionka i arsen. Rozwój badań molekularnych na początku XX wieku pozwolił na identyfikację podłoża genetycznego choroby wykazując obecność mutacji lub rearanżacji genów TP53, MYC, BCL2 w raku drobnokomórkowym i genów EGFR, KRAS, MET, BRAF, NTRK, ROS1, ALK, RET, PIK3CA w raku niedrobnokomórkowym [3]. Odsetek chorych na NDRP o typie innym niż płaskonabłonkowy z mutacją genu dla receptora naskórkowego czynnika wzrostu (ang. epidermal growth factor receptor, EGFR) wynosi 10-15 (u chorych rasy kausaksiej) do ponad 40% (u chorych rasy azjatyckiej) [4]. Delecja w eksonie 19 oraz substytucja w kodonie 858 (L858R) w eksonie 21 stanowi 80-90% mutacji w obrębie domeny kodującej kinazę tyrozynową genu EGFR [4]. Rak płuca objawia się kaszlem, krwiopluciem, bólem w klatce piersiowej, dusznością i/lub chrypką. W przypadku gruczolakoraka często występują przerzuty do mózgu manifestujące się bólem głowy, wymiotami, zaburzeniami pola widzenia, drgawkami lub deficytami neurologicznymi. Po wykonaniu odpowiednich badań laboratoryjnych, obrazowych oraz ocenie histopatologicznej możliwa jest ocena typu histologicznego i stopnia zaawansowania raka. W zależności od stanu ogólnego pacjenta, stadium zaawansowania nowotworu i chorób towarzyszących stosowane są różne metody leczenia. W przypadku raka o niskim stopniu zaawansowania (stadium I, II oraz IIIA) stosuje się leczenie operacyjne często w skojarzeniu z chemioterapią i radioterapią. U chorych w stopniu IIIB terapią z wyboru jest chemioradioterapia, a w przypadku braku możliwości jej zastosowania, postepowanie jest takie jak u chorych na NDRP w stadium uogólnienia. Terapia chorych z odległymi przerzutami (stopień IV) ma na celu zmniejszenie dolegliwości i objawów postępującej choroby oraz wydłużenie czasu życia. W tym celu stosuje się chemioterapię, immunoterapię lub terapię ukierunkowaną molekularnie [5]. Leczenie ukierunkowane molekularnie raka płuca z mutacją genu EGFR możliwe jest dzięki zastosowaniu inhibitorów kinazy tyrozynowej (IKT). IKT hamują wewnątrzkomórkową fosforylację EGFR co prowadzi do zatrzymania różnicowania, proliferacji i angiogenezy komórek. IKT EGFR dzielą się na trzy generacje. Erlotynib oraz gefitynib to odwracalne IKT pierwszej generacji. Są skuteczne w przypadku obecności najczęstszych mutacji w eksonie 19 i 21. Nieodwracalne IKT drugiej generacji, do których należą afatynib i dakomitynib, wykazują szersze spektrum działania. Blokują one przekazywanie sygnałów utworzonych przez receptory ErbB1 (EGFR), ErbB2 (HER2), ErbB3 i ErbB4 oraz mogą być skuteczne w przypadku obecności rzadkich mutacji w eksonach 18, 19, 20 i 21. Możliwe jest nabycie oporności na IKT pierwszej i drugiej generacji. Ozymertynib, nieodwracalny IKT trzeciej generacji, poprzez działanie na komórki z mutacją T790M w eskonie 20 genu EGFR przełamuje oporność na leczenie IKT EGFR starszych generacji, ale może być też stosowany w 1. linii leczenia u chorych na NDRP niezależnie od rodzaju mutacji w eksonach 18-21 genu EGFR [6]. Globalna pandemia COVID-19 stanowi wyzwanie terapeutyczne dla opieki zdrowotnej, zwłaszcza wśród chorych onkologicznych. Analiza retrospektywna z Wuhan wykazała, że ryzyko infekcji COVID-19 było 2,31 razy większe wśród chorych z chorobą nowotworową niż u osób zdrowych. Palenie tytoniu, wiek, płeć męska, stan choroby nowotworowej, zły stan sprawności (≥2 wg skali ECOG) i leczenie hydroksychlorochiną z azytromycyną stanowiły czynniki ryzyka zwiększonej 30-dniowej śmiertelności wśród chorych na COVID-19 [7]. Wizyty w szpitalu podczas pandemii oraz stosowanie leków o działaniu immunosupresyjnym stanowią główne czynniki sprzyjające infekcji COVID-19 u chorych na nowotwory płuc [8]. Badanie przeprowadzone w Chinach, wykazało, że chorzy na NDRP powyżej 60 roku życia są szczególnie narażeni na infekcję COVID-19 i cięższy przebieg choroby. Wiele objawów ze strony układu oddechowego w COVID-19 tj. duszność, kaszel, gorączka pokrywa się z objawami raka płuca. Stwarza to trudność w diagnostyce różnicowej pomiędzy tymi dwoma jednostkami chorobowymi. Rozpoznanie COVID-19 jest zwykle dokonywane na podstawie wywiadu klinicznego i testu PCR i/lub testu antygenowego w próbce z wydzieliny jamy nosowo-gardłowej. Pomocne jest także rozpoznanie typowych zmian widocznych w tomografii komputerowej klatki piersiowej. U 75% chorych obecne są wieloogniskowe zmętnienia typu matowego szkła z predylekcją do płatów dolnych [9]. Badanie przeprowadzone w Nowym Jorku wśród chorych na raka płuca ze współistniejącą infekcją SARS-CoV2 wykazało konieczność hospitalizacji u 62% pacjentów, z czego 21% wymagało hospitalizacji na OIOM. Spośród 102 chorych biorących udział w badaniu, 25% zmarło. Przeżycie było w większym stopniu zależne od współwystępowania POChP (przewlekłej obturacyjnej choroby płuc) i palenia tytoniu niż histologii guza lub ekspresji PD-L1 (ang. programmed death ligand 1) na komórkach nowotworowych [10].
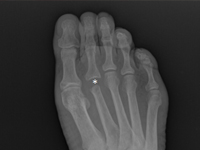
Przykład postępowania w przypadku guza II kości śródstopia pierwotnie podejrzewanego jako przerzut raka pęcherzykowatego tarczycy 40 i 20 lat po całkowitej tyroidektomii
Example of management of metatarsal bone II tumor originally suspected of having metastatic thyroid follicular cancer 40 and 20 years after total thyroidectomy
GinekologiaZnanych jest wiele przyczyn wywołujących dyskomfort i zmiany guzowate w okolicy śródstopia i przodostopia. Obejmują one urazowe uszkodzenia tkanek miękkich i kości (np. rozerwanie płytki podeszwowej, zapalenie trzeszczek palucha, zapalenia stawów, złamania zmęczeniowe, złamanie Freiberga), choroby ścięgien (np. tendinoza, zapalenie pochewki ścięgna, zerwanie ścięgna), nienowotworowe zmiany tkanek miękkich (np. ganglion, zapalenie kaletki, ziarniniak, nerwiak Mortona), oraz rzadziej nowotwory i ich przerzuty do tkanek miękkich i kości [1]. Ogniskowe zmiany kości są często przypadkowym wynikiem obrazowania. Alternatywnie mogą być przyczyną bólu, wyczuwalnej masy lub złamania patologicznego [2].Najczęściej chorzy wiążą te objawy z urazem. W rzeczywistości uraz jedynie zwraca uwagę na chore miejsce, ale nie powoduje powstania guza. [5] We wszystkich tych przypadkach, zwłaszcza w początkowym okresie, trafne rozpoznanie jest kluczowe, aby ustalić dalszą diagnostykę różnicową i strategię leczenia, dlatego w konfrontacji z ogniskową zmianą kostną należy przestrzegać logicznego algorytmu postępowania. Najpierw powinno się zapewnić opis zmiany w korelacji z wiekiem pacjenta, lokalizacją, rodzajem kości, zajęciem korówki, reakcjami okostnej, stanem sąsiadującej tkanki miękkiej. W tym celu należy wykonać rtg zajętego obszaru w dwóch projekcjach z sąsiadującymi stawami. Pogłębienie diagnostyki uzyskujemy poprzez badanie TK, oceniające zaawansowanie zmian kostnych i MRI, infiltrację sąsiadujących tkanek miękkich . Jeżeli badania obrazowe wykażą większe zaawansowanie choroby, istotnym elementem diagnostycznym jest uzyskanie materiału do badania patomorfologicznego, pobranego w trakcie biopsji otwartej lub oligobiopsji i ustalenie rozpoznania histologicznego [11]. W przypadku potwierdzenia procesu nowotworowego konieczne zawsze jest wykonanie badania RTG/TK klatki piersiowej, USG/TK jamy brzusznej, a nawet PET celem wykluczenia przerzutów [5]. Drugi etap wdrożonego algorytmu nakazuje zaplanować leczenie w oparciu o odpowiedzi na następujące pytania: - Czy zmiana może być normalnym wariantem, czyli „zostaw mnie w spokoju, nie dotykaj”, uszkodzenie łagodnego typu, nie wymagające dalszego obrazowania i zaopatrzenia, a tylko obserwacji? [3] - Czy zmiana ma cechy sugerujące agresywną naturę, a wtedy czy konieczne jest dalsze obrazowanie, którą technikę najlepiej zastosować, czy wymagana jest biopsja zmiany i zaawansowane leczenie? [4]. Niejednorodność obrazu klinicznego niezidentyfikowanych ogniskowych zmian guzowatych w okolicy śródstopia i przodostopia, różnorodność dostępnych metod diagnozowania nie ułatwiają zadania, zarówno na etapie stawiania wstępnego rozpoznania, jak i podczas komunikacji między członkami zespołu interdyscyplinarnego, który niejednokrotnie powinien zająć się leczeniem. Celem tego artykułu jest przedstawienie podobnej sytuacji na przykładzie przypadku guza nasady dalszej II kości śródstopia, podejrzewanego o późny, odległy przerzut raka tarczycy, nigdy nie potwierdzony w dalszych badaniach oraz sugestii dotyczących postępowania diagnostyczno-terapeutycznego. Rak pęcherzykowy tarczycy (FTC - Follicular Thyroid Carcinoma) stanowi 10-20% wszystkich nowotworów tarczycy. Jest to drugi co do częstości spotykany rak tarczycy [6], a przerzuty do kości śródstopia i palców są wyjątkowo rzadkie.
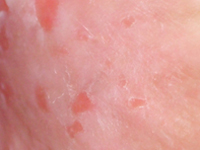
Radykalna radioterapia konformalna w leczeniu nawracającej, pozasutkowej postaci choroby Pageta - opis przypadku.
Radical conformal radiotherapy in treatment of recurrent, extramammary Paget disease - case report.
InternaChoroba Pageta jest rzadkim procesem nowotworowym wywodzącym się z gruczołów apokrynowych i ekrynowych skóry [1]. Wyróżnia się postać sutkową (ang. mammary Paget disease, MPD) i postać pozasutkową (ang. extramammary Paget disease, EMPD), stanowiące odpowiednio 90% i 10% wszystkich przypadków choroby Pageta [2]. Częstość występowania EMPD w populacji europejskiej szacuje się na 0,7 na 100 000 osób/rok [3]. EMPD częściej rozpoznawana jest u kobiet, szczególnie rasy kaukaskiej, między 50 a 80 r.ż. [4], u których przeważnie lokalizuje się na sromie i kroczu oraz w okolicy okołoodbytniczej, zaś u mężczyzn na prąciu i worku mosznowym [5,6]. Objawy choroby są mało charakterystyczne, co w większości przypadków utrudnia postawienie właściwego rozpoznania i tym samym wydłuża czas do rozpoczęcia leczenia. Jedynie badanie histopatologiczne wyciętej zmiany chorobowej pozwala na postawienie prawidłowej diagnozy oraz ocenę stopnia inwazyjności procesu [6]. Podstawową metodą leczenie pozostaje radykalne leczenie chirurgiczne [7]. Z uwagi na wysoki odsetek nawrotów [4,8] część chorych wymaga leczenia uzupełniającego [6]. W przypadkach niekwalifikujących się do operacji stosuje się miejscową lub systemową chemioterapię lub radioterapię [9,10].Z uwagi na bardzo rzadkie występowanie choroby, brak ustalonych schematów leczenia, obserwowane niepowodzenia i podejmowane kolejne próby interwencji chirurgicznych, prezentowany przypadek stanowi przykład możliwości leczenia EMPD z użyciem promieniowania jonizującego.